Elettrolisi
|
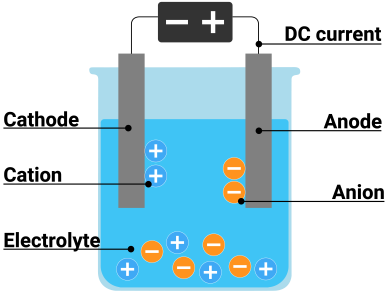
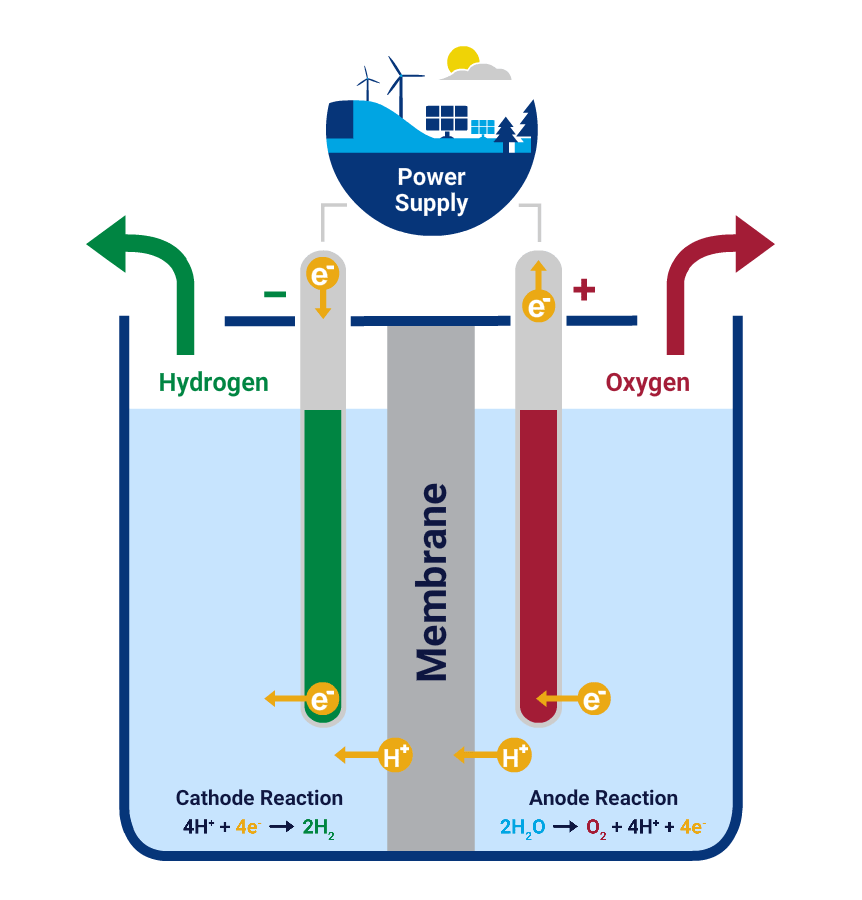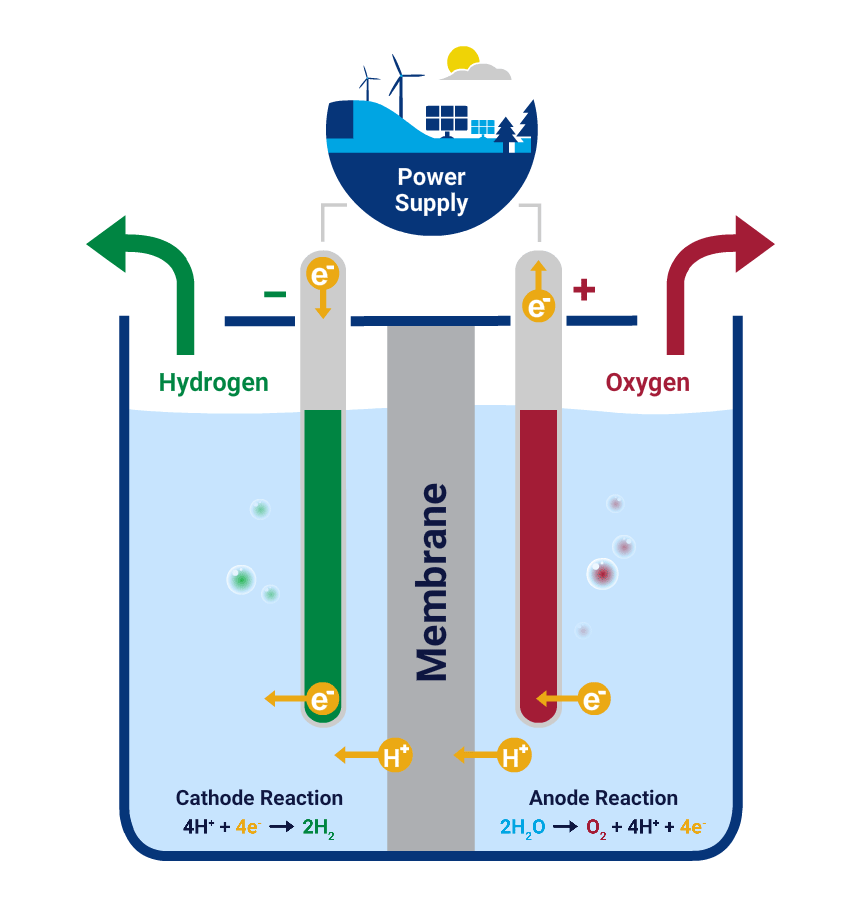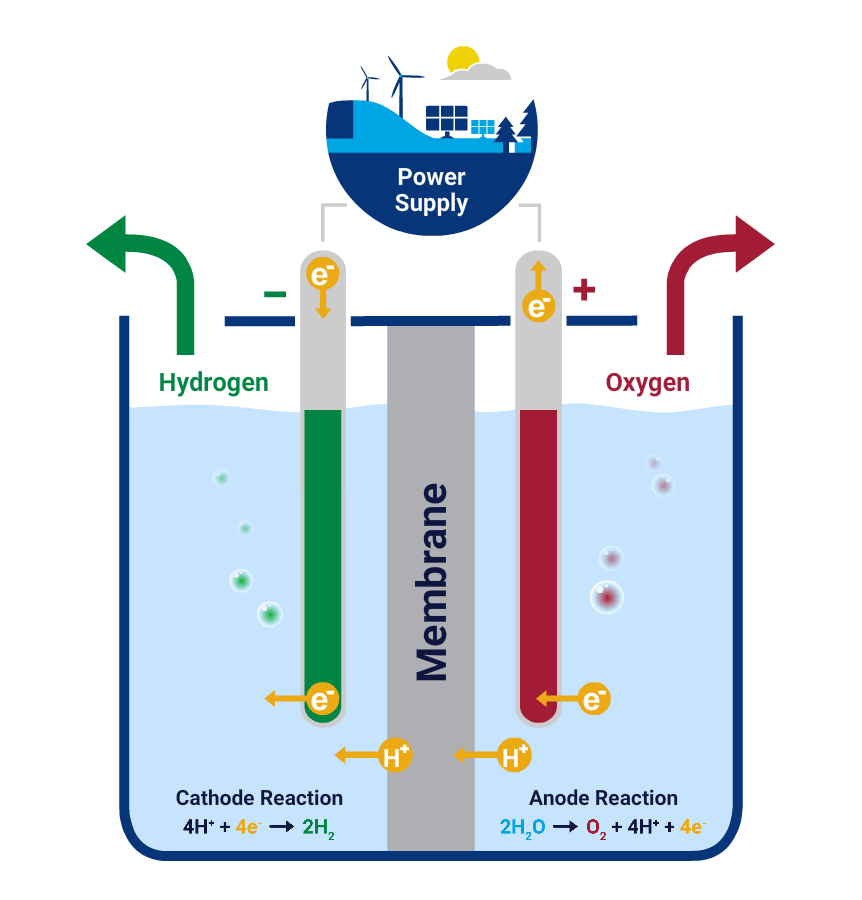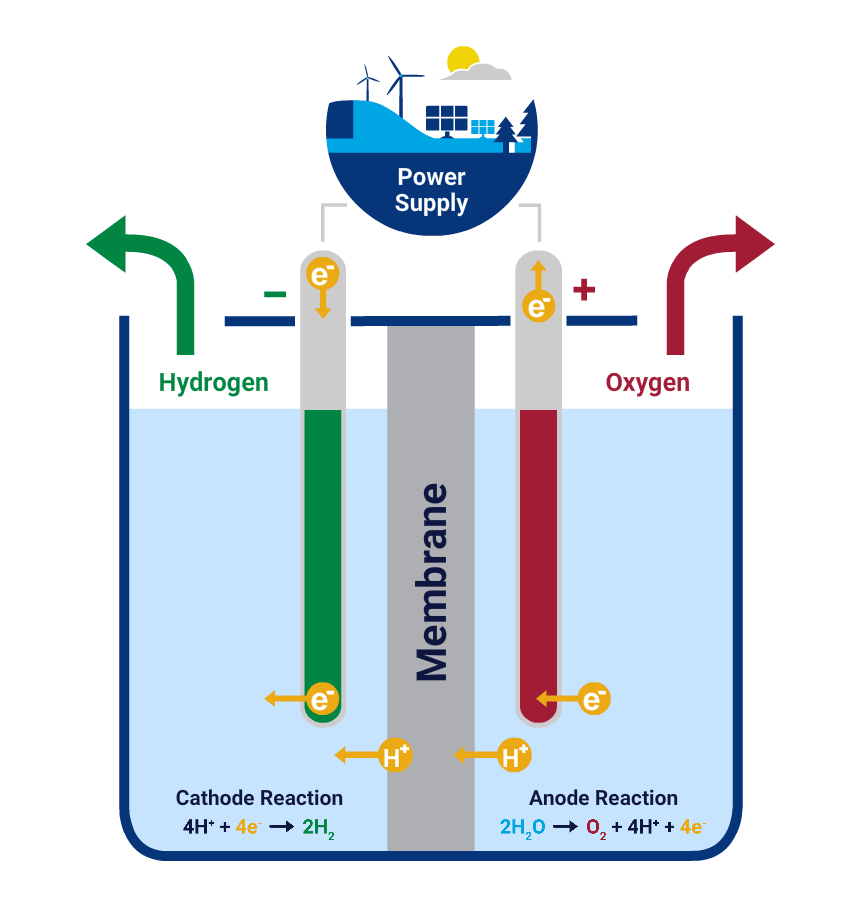
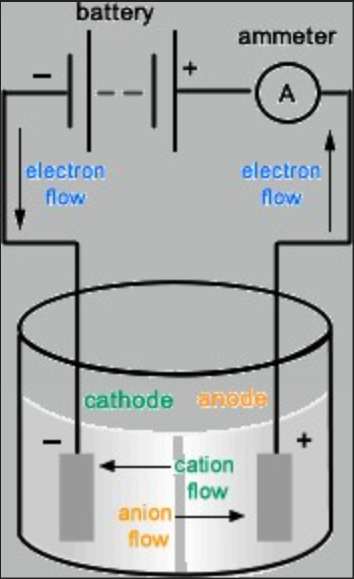
Quando un oggetto in ferro viene esposto all'aria e all'umidita' viene automaticamente sottoposto ad un processo di ossidazione che a lungo termine andra' a formare la ruggine. Durante tale processo lo strato di ruggine aumenta progressivamente di volume e di conseguenza, con il passare del tempo la ruggine si "spezza" e cade via andandosi a formare nuovamente sulla parte di metallo che si e' scoperta e questo a lungo andare causa una perdita progressiva della superficie del metallo sano. La ruggine quindi e' un processo chimico naturale e spontaneo mentre l'elettrolisi e' un processo chimico che grazie alla corrente elettrica in una soluzione acquosa trasforma l'energia elettrica in energia chimica invertendo il processo. In poche parole si riduce l'ossido di ferro (cioe' la ruggine) grazie all'azione degli ioni di idrogeno che si separano dal catodo ( - ) e vengono attirati dall'anodo ( + ). Quindi gli ioni positivi (cationi) migreranno verso l'elettrodo negativo (catodo) e gli ioni negativi (anioni) verso l'elettrodo positivo (anodo). L'elettrolisi non causa danni al metallo.
|
|
La macchina per l'elettrolisi e' composta fondamentalmente dai seguenti componenti:
Il tempo richiesto dal processo dipende da:
Consigli per la sicurezza:
|
Sorgente DC
|
Partiamo parlando della sorgente DC. E' possibile utilizzare anche una batteria ma e' vivamente consigliato un alimentatore. La tensione ideale e' compresa tra i 6V e i 24V (normalmente si utilizzano 12V, la tensione ideale e' di 24V, oltre la quale non si ottengono benefici). L'alimentatore piu' adatto e' quello per ricaricare le batterie dei veicoli, abbiamo bisogno di una modesta quantita' di corrente (5-10A). Sarebbe ottimo se l'alimentatore possiede un amperometro integrato, in questo modo possiamo tenere sotto controllo lo stato del processo, in caso contrario possiamo munirci di un multimetro.
Prestate attenzione a non mandare in corto circuito l'alimentatore (per esempio facendo toccare le pinze oppure gli elettrodi stessi). |
Elettrodi
|
L'elettrodo negativo (catodo) e' l'oggetto stesso che dobbiamo preservare. L'elettrodo positivo (anodo) viene anche chiamato elettrodo sacrificale (o di scarto) poiche' dopo svariati lavaggi si disintegrera' piano piano riducendosi sempre di piu' fino a quando sara' necessaria una sostituzione con un nuovo elettrodo. La scelta del materiale per l'elettrodo positivo va fatta con cura:
|
Ecco qualche consiglio per gli elettrodi:
- La grandezza dell'anodo da utilizzare deve superare l'area dell'oggetto da preservare
- L'oggetto deve essere circondato da due o piu' elettrodi positivi in modo da effettuare il processo in maniera omogenea.
- Le pinze attaccate agli elettrodi non devono essere immerse nella soluzione altrimenti si consumeranno!
- Gli elettrodi positivi non devono toccare l'oggetto da preservare (elettrodo negativo) altrimenti si va a creare un corto circuito.
- Per diminuire il tempo dell'elettrolisi, posizionate gli elettrodi positivi il piu' vicino possibile all'oggetto da preservare (se avete un multimetro a portata di mano, impostatelo per misurare la corrente e noterete che avvicinando gli elettrodi positivi all'oggetto la corrente aumentera').
- Ogni 3-4 ore controllate lo stato degli elettrodi positivi; se si sono incrostati l'efficienza dell'elettrolisi va a calare, quindi spazzolateli con la spazzola di metallo. Se dovete lasciare l'elettrolisi accesa di notte e le barre si incrostano non succede niente, al massimo il processo e' meno efficiente e richiede piu' tempo per il completamento.
Elettrolita
|
Produrre l'elettrolita e' molto semplice, basta un po' di acqua (l'ideale sarebbe quella demineralizzata/distillata) e il relativo solvente. Non c'e' una quantita' precisa da utilizzare, solitamente si utilizza la regola: "1 cucchiaio di solvente per ogni litro di acqua".
Per essere certi della quantita' da utilizzare possiamo aiutarci con un multimetro (oppure, se presente, l'amperometro integrato dell'alimentatore); basta impostarlo per effettuare la misurazione della corrente (utilizzate un fondo scala adeguato tipo 5-10A) e poi lo colleghiamo tra la pinza positiva e l'elettrodo positivo. Successivamente aggiungete il solvente, noterete che il valore della corrente misurata salira' progressivamente a mano a mano che ne aggiungete altro; raggiungete almeno 2A poi potete fermarvi. Durante la fase iniziale (prima ora) la corrente deve essere compresa tra i 2A-6A. Durante il processo la ruggine iniziera' a togliersi e questo comportera' una migliore conduzione con l'oggetto in ferro e di conseguenza la corrente aumentera' ulteriormente. Se all'inizio del processo la corrente e' bassa o vicina allo zero, allora c'e' qualcosa che non va (collegamenti errati o scadenti, elettrolita non adatto oppure presente in basse concentrazioni). Ecco una lista di solventi:
|